تیتراسیون روشی آزمایشگاهی است برای تجزیهوتحلیل شیمیایی کمی و تعیین غلظت آنالیت.
در این روش آنالیت مادهای است که باید آنالیز شود. همچنین به معرف، تیترانت یا تیتراتور میگویند و از آن بهعنوان محلول استاندارد با غلظت و حجم مشخص استفاده میشود.
تیترانت با محلولی از آنالیت واکنش میدهد تا غلظت آنالیت را مشخص کند.
در ادامه به روش انجام تیتراسیون و انواع آن اشاره میشود.
تعریف تیتراسیون به زبان ساده
تیتراسیون یا تیترسنجی عبارت است از تکنیک تجزیهوتحلیل کیفی شیمیایی که برای محاسبه غلظت یک آنالیت معین در مخلوط انجام میشود. از تیتراسیون برای تعیین غلظت یک نمونه نامعلوم استفاده میشود. تیتراسیون (به انگلیسی Titration) روشی مهم در شیمی تجزیه است و گاهی بهعنوان آنالیز حجمی شناخته میشود.

روش تیتراسیون
روش تیتراسیون با تهیهی یک تیترانت که محلولی استاندارد با حجم و غلظت مشخص است، شروع میشود. سپس واکنش تیترانت با آنالیت آغاز میشود تا وقتیکه به نقطه پایانی برسد. در اینجا می توان غلظت آنالیت را با اندازهگیری مقدار تیتر مصرفی مشخص کرد. البته برای مشخص کردن غلظت مجهول یک محلول، از روش دیگری به نام روش استوکیومتری نیز می توان استفاده کرد.
نکته مهم در روش تیتراسیون این است که تیترانت و آنالیت هر دو باید بهصورت مایع (محلول) باشند. اگر مواد جامد بودند، از حلالهایی مانند اسید استیک یا اتانول برای حل کردن آنها میتوان استفاده کرد. اگر آنالیتها غلیظ باشند نیز باید آنها را رقیق کرد تا دقت آزمایش بالاتر برود.
توجه به این نکته نیز ضروری است که در اکثر واکنشهای تیتراسیون (بهجز اسید-باز)، pH محیط واکنش باید ثابت باشد. به همین منظور برای ثابت ماندن pH، از یک محلول بافر در این واکنشها استفاده میشود. روشهای تیتراسیون، شامل آنالیز وزنی، تحلیل حجمی، طیفسنجی، تجزیهوتحلیل احتراق میباشد.
کلیک کنیم: خرید اینترنتی انواع ظروف شیشه ای آزمایشگاهی
انواع تیتراسیون
واکنشهای تیتراسیون را بر اساس نوع واکنشها، میتوان به گروههای زیر تقسیمبندی کرد.
- اسید و باز
- برگشتی
- ردوکس
- بارش
- کمپلکسومتری
- مستقیم
- وزنی
- رسوبی
در ادامه هر گروه را بهصورت مختصر توضیح میدهیم.
-
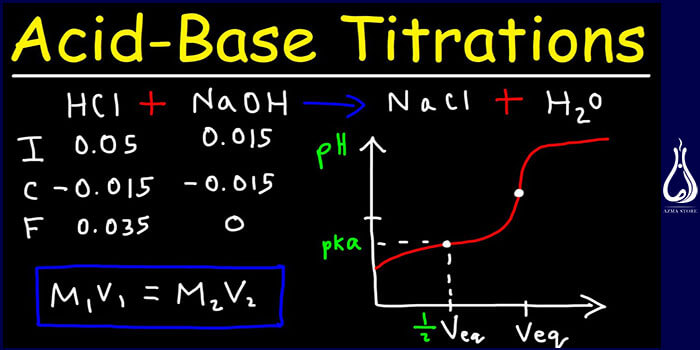
تیتراسیون اسید و باز
در این روش یک نشانگر pH مناسب به محفظه تیتراسیون اضافه میشود. این نشانگر، نشاندهنده pH نقطه هم ارزی میباشد. واکنش کلی در این تیتراسیون، خنثی شدن اسید و باز در زمان مخلوط شدن در محلول است. فنل فتالئین و متیل اورانژ، از شاخصهای pHهستند که بهصورت متداول در این واکنشها مورد استفاده قرارمیگیرند. بدینصورت که شناساگرها با تغییر رنگ محلول، پایان واکنش را نشان میدهند. فرایند اسید سنجی عبارت است از تعیین قدرت یک اسید با استفاده از محلول استاندارد یک باز.
در این واکنشها اسیدها را برحسب میزان تفکیک، به دو گروه تقسیمبندی میکنند(قوی و ضعیف). درصورتیکه محلول اسیدی با غلظت مشخص در برابر یک باز قوی تیتر شود، هنگام پایان واکنش خنثیسازی، می توان غلظت اسید را محاسبه کرد.
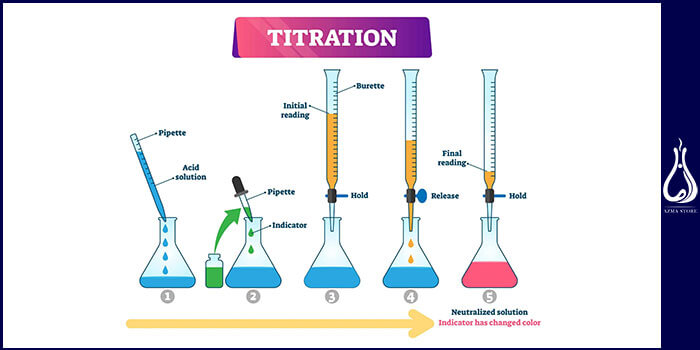
روش آزمایش تیتراسیون اسید و باز
محلول پایه، محلولی است که غلظت مشخصی دارد. حجم مورد نیاز از آن را به یک پیپت و فلاسک انتقال میدهند. سپس اسید با غلظت مجهول به همراه شناساگر را در بورت میریزند. محتویات بورت باید قطره قطره ریخته شود و با باز واکنش دهد. تغییر رنگ محلول (به دلیل وجود شناساگر)، نشاندهنده ی پایان واکنش میباشد.
شاخصی که استفاده میشود، میتواند فنل فتالئین باشد. فنل فتالئین در محلول بازی به رنگ صورتی ولی در محلول اسیدی بیرنگ میباشد. پس نقطه پایان واکنش، لحظهای است که محلول صورتیرنگ، بیرنگ شود.
انتخاب شاخص
نکته حائز اهمیت این است که در صورت ضعیف بودن اسید، تشخیص نقطه پایانی بسیار مشکل خواهد بود. برای حل این مشکل، از نمک اسید ضعیف در برابر اسید قوی استفاده میکنند. به دلیل اینکه باز مزدوج اسید ضعیف، یک باز قوی است.
کلیک کنیم: خرید آب مقطر قیمت مناسب

-
تیتراسیون برگشتی (غیرمستقیم یا معکوس)
تیتراسیون برگشتی بیشتر در واکنش اسیدـباز مورد استفاده قرار میگیرد. همچنین زمانی که غلظت مولی یک واکنشدهنده اضافی مشخص باشد از این روش میتوان استفاده کرد.
برای تعیین غلظت آنالیت، از واکنش دادن آن با مقدار مشخصی از معرف اضافی استفاده میشود. سپس معرف اضافی باقیمانده با معرف دوم تیتر میشود.
در این واکنشها، نتیجه نهایی تیتراسیون دوم، نشاندهنده مقدار مصرفی از معرف اضافی در تیتراسیون اول میباشد که امکان محاسبه غلظت آنالیت اصلی را میدهد.
کلیک کنیم: خرید ارلن با کیفیت
-
تیتراسیون اکسایش-کاهش (ردوکس)
تیترسنجی ردوکس، بهصورت فرایند کاهش اکسیداسیون تعریف میشود و به آن واکنش اکسیداسیون- احیا نیز میگویند. این نوع تیتراسیون یک واکنش شیمیایی است که در حالت کلی با انتقال الکترون در یونهای واکنشدهنده محلولهای آبی اتفاق میافتد. درصورتیکه الکترونها بین یونهای واکنشدهنده در محلول آبی منتقل شوند، واکنش شیمیایی اتفاق میافتد.
مثلاً تیتراسیون بین محلول اسید اگزالیک و محلول اسیدی شده KMnO4 (پتاسیم پرمنگنات) یک تیتراسیون ردوکس میباشد.
KMnO4 + H2SO4 → K2SO4 + MnSO4 + H2O + CO2
تیترسنجیهای پایه به دست آمدن غلظت مجهول یک عامل کاهنده با اکسنده میباشد. عوامل اکسنده، در برابر عوامل احیاکننده و عوامل کاهنده در برابر عوامل اکسیدکننده قوی تیتر میشوند.
نکتهی جالبتوجه در واکنشهای ردوکس این است که در این واکنشها ما احتیاجی به شناساگر نداریم. مانند تیترسنجی یدومتری و پرمنگانومتری. در این واکنشها یکی از واکنشدهندهها بهعنوان شناساگر عمل میکنند و رنگ آنها را باحالتهای اکسیدکننده تغییر میدهند.
کلیک کنیم: نحوه شستشوی ظروف آزمایشگاهی {از ظروف نو تا ظروف شیمی آلی}

-
تیتراسیون بارش
تیتراسیون بارش هنگام تشکیل یک رسوب نامحلول در زمان تماس دو ماده واکنشدهنده اتفاق میافتد.
مثلاً هنگامیکه محلول نیترات نقره با محلول تیوسیانات آمونیوم یا محلول کلرید سدیم واکنش میدهد، رسوب سفیدی از کلرید نقره یا تیوسیانات نقره به وجود میآید.
AgNO3 + NaCl → AgCl + NaNO3
AgNO3 + NH4CNS → AgCNS + NH4NO3
-
تیتراسیون کمپلکسومتری
تیتراسیون کمپلکسومتری عبارت است از ایجاد یک کمپلکس بین آنالیت و تیتراتور پایهای برای تیترسنجیهای کمپلکس سنجی. یکی از متداولترین عوامل کیلیت کننده در این روش، EDTA است.
–Ag+ + 2CN– → [Ag(CN)2]
Hg2+ + 2SCN– → Hg(SCN)2

-
تیتراسیون مستقیم
یکی از روشهای تیترسنجی پایه میباشد که در آن، ترکیب با غلظت مشخص با ترکیب مجهول واکنش میدهد. در این روش، ترکیب مجهول با ترکیب شناخته شده مستقیماً واکنش میدهد و معرفهای اضافی اضافه نمیشود. (مانند روش برگشتی).
-
تیتراسیون وزنی
تیتراسیون وزنی روشی است که در آن مقدار تیتر مورد نیاز بر اساس وزنی که باید برای رسیدن به نقطه پایانی اضافه شود، مشخص میشود.
-
رسوبی
تیتراسیون رسوبی یکی از قویترین تکنیکها است و نقطه پایانی آن بر اساس تغییر ناگهانی در خواص فیزیکی محلول اتفاق میافتد.

فرمول تیتراسیون
مولاریته عبارت است از غلظت محلول به تعداد مول املاح در لیتر محلول.
اگر تیترانت و آنالیت نسبت مول 1 به 1 داشته باشند، فرمول مولاریته (M) اسید ضرب در حجم (V) اسید = مولاریته (M) باز ضرب در حجم (V) باز میباشد.
MAVA = MBVB
مثال:
اگر 35 میلیلیتر محلول HCl با مولاریته 1.25 داشته باشیم، غلظت 25 میلیلیتر محلول NaOH را محاسبه نمایید.
NaOH + HCl → NaCl + H2O
پاسخ: با توجه به معادله بالا، نرخ مول اسید و باز یکبهیک مشخص شده است. بر طبق فرمول تیتراسیون، میتوان غلظت نامعلوم را به دست آورد.
MAVA = MBVB
M x 25 = 35 x 1.25
MB = 1.75
منحنی تیتراسیون
منحنی تیتراسیون، عبارت است از منحنی که مختصات X آن حجم تیتر اضافه شده از ابتدای تیتراسیون و مختصات Y آن غلظت آنالیت در مرحله مربوط به تیترسنجی را نشان میدهد.
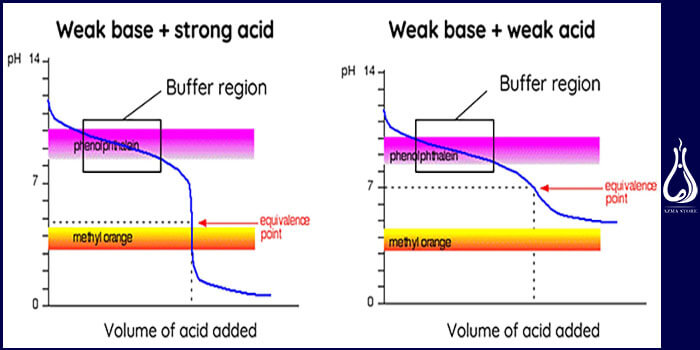
در روش اسید-باز، مختصات Y معمولاً نشاندهنده pH محلول و منحنی قدرت اسید و باز است. درصورتیکه اسید و باز قوی باشند، منحنی نسبتاً صاف و در نزدیکی نقطه هم ارزی بسیار شیبدار خواهد بود. بنابراین حتی تغییری کوچک در حجم تیتراتور در نزدیکی نقطه هم ارزی، میتواند منجر به تغییر زیادی در pH شود.
کاربرد تیتراسیون
بهطورکلی ار روش تیتراسیون برای به دست آوردن غلظت نامشخص یک آنالیت با غلظت مشخص یک محلول زمانی که شاخص وجود داشته باشد، استفاده میشود.
همچنین از روش تیتراسیون می توان برای ارائه خلوص نمونهها و محاسبات مربوط به pH نیز استفاده کرد.
آیا نقطه پایان و نقطه هم ارزی یکسان هستند؟
میدانیم که نقطه هم ارزی توسط استوکیومتری واکنش تعیین میشود و نقطه پایان تنها تغییر رنگ شناساگر را نشان میدهد. بنابراین نقطه پایان و نقطه هم ارزی یکسان نیستند.
(از فنل فتالئین بهعنوان یکی از رایجترین شاخصها استفاده میشود.)
جمعبندی
تیتراسیون عبارت است از یک روش آزمایشگاهی برای مشخص کردن غلظت ماده مجهول، به کمک یک مادهی مشخص.
علاوه بر آن، از این روش برای محاسبات مربوط به pH و ارائه خلوص نمونهها نیز میتوان استفاده کرد.
واقعا مقاله هاتون حرف نداره. کلی مطالب آموزشی بدرد بخور داره
آتریسا جان، خوشحالیم که تلاش های ما مورد لطف شما قرار گرفت.